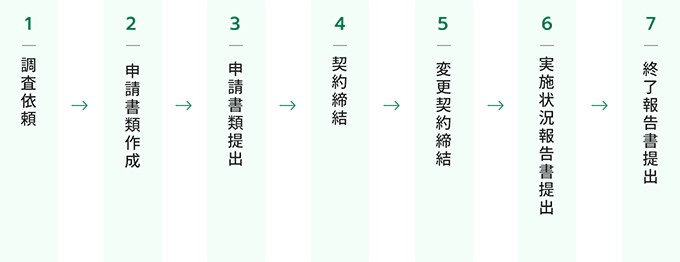
1調査依頼
調査実施について診療科部長の了承を得て下さい。診療科ごとの契約となります。
当院で採用されている医薬品及び医療機器が対象です。採用前の申請はできませんので、採用後にご申請下さい。
登録のみの場合も契約が必要となります。
2申請書類作成
申請書類は本ページからダウンロードできます。提出前に内容を確認しますので、必要事項を記載し、添付資料とともに臨床研究課担当者へ電子にて送付して下さい。
3申請書類提出
必要箇所に押印後、臨床研究課に提出して下さい。
契約書の締結日は空欄にして下さい。
申請は、随時受け付けております。
4契約締結
病院長の承認を得た後、契約を締結します。(※ 調査開始は原則として契約締結後となります。)
5変更契約締結
原契約の予定症例数を上回る場合や期間延長を行う場合は、変更申請書・変更契約書を作成し、臨床研究課担当者へ電子にて送付して下さい。
原契約の契約期間が切れる前に、変更契約を締結して下さい。
6実施状況報告書提出
契約中の調査について、調査票が固定された場合は、1年を目安として実施状況報告書を提出して下さい。実施状況報告書に基づいて請求書を発行いたします。
7終了報告書提出
調査が終了した場合は、必ず契約期間内に終了報告書を提出して下さい。
提出書類
新規申請
| 書類名 | 医薬品 | 医療機器 |
|---|---|---|
| 1. 製造販売後調査実施依頼書 | Excel | Excel |
| 2. 製造販売後調査実施申請書 | ||
| 3. 製造販売後調査実施契約書 | Word | Word |
| 4. 製造販売後調査実施契約書3者契約用 | Word | Word |
| 5. 調査実施計画書または調査実施要綱 | ||
| 6. 調査票見本または入力画面サンプル | ||
| 7. 調査薬若しくは調査機器の添付文書または概要書 |
変更申請
| 書類名 | 医薬品 | 医療機器 |
|---|---|---|
| 1. 製造販売後調査変更申請書 | Excel | Excel |
| 2. 製造販売後調査変更契約書 |
実施状況報告
| 書類名 | 医薬品 | 医療機器 |
|---|---|---|
| 1. 製造販売後調査実施状況報告書 | Excel | Excel |
| 2. 調査票の写し(医師署名頁、初回投与(使用)日のわかる頁のみ) |
終了報告
| 書類名 | 医薬品 | 医療機器 |
|---|---|---|
| 1. 製造販売後調査終了報告書 | Excel | Excel |
| 2. 調査票の写し(医師署名頁、初回投与(使用)日のわかる頁のみ) |
副作用等調査
| 書類名 | 様式 | |
|---|---|---|
| 1. 副作用等報告調査依頼書 | Excel | |
| 2. 副作用等報告調査実施契約書 | Word | |
| 3. 副作用等報告調査終了報告書 | Excel | |
調査に要する経費
調査報告書作成経費は1症例1報告あたりの単価に症例数を乗じます。但し、複数の報告書を作成する場合は、報告書の冊数を積算します。
| 調査種別 | 単価(税別) |
|---|---|
| 使用成績調査 | 20,000円 |
| 特定使用成績調査 | 30,000円 |
| 副作用等報告調査 | 10,000円 |
手続きに関する問い合わせ先
病院事務部 臨床研究課
- TEL 0798(45)6094
-
MAIL




